一个原子的价层电子分布不会是(n-1)d ns
ns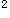 ,是因为这种分布违背了( )。
,是因为这种分布违背了( )。
 ns
ns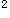 ,是因为这种分布违背了( )。
,是因为这种分布违背了( )。 正确答案:
B
答案解析:
【解析】d轨道共有5个,按不相容原理的要求可以容纳10个电子而达到全满,s轨道只有一个,可以容纳2个电子而达到全满,(n-1)d ns
ns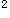 。的分布方式很显然与洪特规则的特例不一致,所以答案(B)是正确的,应该采取(n-1)d
。的分布方式很显然与洪特规则的特例不一致,所以答案(B)是正确的,应该采取(n-1)d ns
ns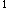 的方式分布。
的方式分布。
【点评】原子核外电子分布要遵循能量最低原理、不相容原理和洪特规则。能量最低原理是指核外电子应尽可能占据能量最低的原子轨道;不相容原理是指在同一个原子中不可能有四个量子数完全相同的两个电子,其重要推论就是一个原子轨道只能容纳两个电子;洪特规则是指在能量相同的简并轨道(即同种原子轨道)中,电子应尽可能分占轨
道、自旋平行。洪特规则还有一个特例,就是一种原子轨道应尽可能处于全满、半满或全空状态。
 ns
ns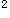 。的分布方式很显然与洪特规则的特例不一致,所以答案(B)是正确的,应该采取(n-1)d
。的分布方式很显然与洪特规则的特例不一致,所以答案(B)是正确的,应该采取(n-1)d ns
ns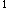 的方式分布。
的方式分布。【点评】原子核外电子分布要遵循能量最低原理、不相容原理和洪特规则。能量最低原理是指核外电子应尽可能占据能量最低的原子轨道;不相容原理是指在同一个原子中不可能有四个量子数完全相同的两个电子,其重要推论就是一个原子轨道只能容纳两个电子;洪特规则是指在能量相同的简并轨道(即同种原子轨道)中,电子应尽可能分占轨
道、自旋平行。洪特规则还有一个特例,就是一种原子轨道应尽可能处于全满、半满或全空状态。
